医疗器械网页设计 国家药品监督管理局实施医疗器械注册电子申报有关事项的公告(2019年第46号)
关于推进医疗器械注册电子申报的公告
(2019年第46号)
为推进中共中央办公厅、国务院办公厅《关于加强审评审批机制改革引导药品医疗器械创新的意见》(厅字〔2017〕42号),实现医疗器械注册办理的电子申报医疗器械网页设计,国家药品监督管理局组织研发了医疗器械注册电子申报信息化平台(eRPS)。现将实行医疗器械注册电子申报有关事项公告如下:
一、适用范围
现在医疗器械网页设计,eRPS系统业务范围为国家药品监督管理局医疗器械注册事项,包括境内第三类和进口第二、三类医疗器械注册、注册变更、延续注册,第三类高风险医疗器械临床实验审批,以及医疗器械说明书修改告知、医疗器械注册及许可事项变更审查、创新医疗器械特别审查等。
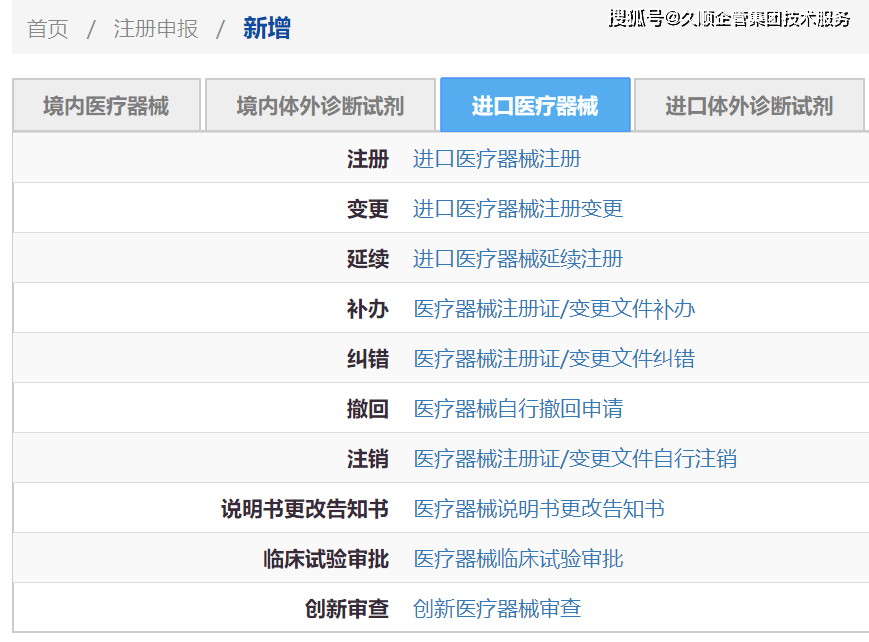
进口第一类医疗器械备案,注册证及更改文件的办理、纠错、自行注销、自行中止,医疗器具注册指定检测等事项暂不包括在eRPS系统业务范围之内。
二、时间安排
(一)CA申领
自2019年5月起,医疗器械注册办理人、注册人申请eRPS系统配套使用的数字认证证书(CertificateAuthority,CA)。具体办理通知请关注国家药品监督管理局医疗器械技术审评中心网站()。
(二)系统启用
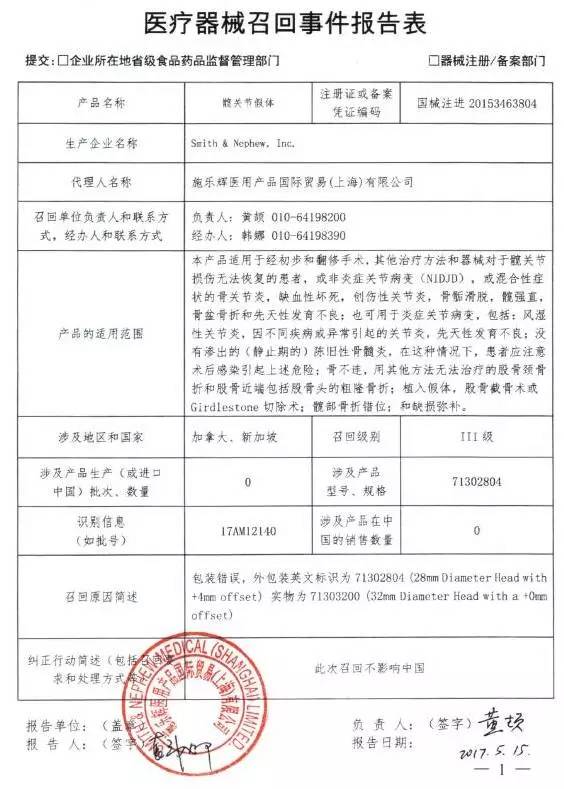
2019年6月24日,正式推出eRPS系统。医疗器械注册办理人、注册人可进行线上医疗器械注册电子申报,无需递交纸质资料。同时,国家药品监督管理局保留纸质资料的提交途径。
2019年10月31日前,纸质资料递交按照现行医疗器械、体外检测试剂注册申报资料规定进行。
2019年11月1日起,纸质资料递交应当依照《医疗器械注册办理电子提交技术指南(实行)》的规定,与电子申报目录形式一致。
详细事项及规定见附件《医疗器械注册电子申报信息化平台(eRPS)启用说明》。
特此公告。

国家药监局2019年5月29日
附件
识别二维码即可查看
附件:医疗器械注册电子申报信息化平台(eRPS)启用说明

转载原创文章请注明,转载自设计培训_平面设计_品牌设计_美工学习_视觉设计_小白UI设计师,原文地址:http://www.zfbbb.com/?id=6320





